近日,南昌医学院柔性引进人才张青锋教授在国际一流学术期刊《Nature Communications》(自然·通讯)上发表了题为“Epigenetically conferred ring-stage survival inPlasmodium falciparumagainst artemisinin treatment”的研究成果,揭示了疟疾病原体(疟原虫)对青蒿素产生耐药性的全新机制。张青锋教授长期致力于研究寄生虫与人体宿主互作及其致病的分子机制,为文章的第一通讯作者,南昌医学院为通讯单位之一。南昌医学院基础医学院陈璇博士为共同第一作者,参与了本项研究的完成。

原文链接:https://www.nature.com/articles/s41467-025-62479-2
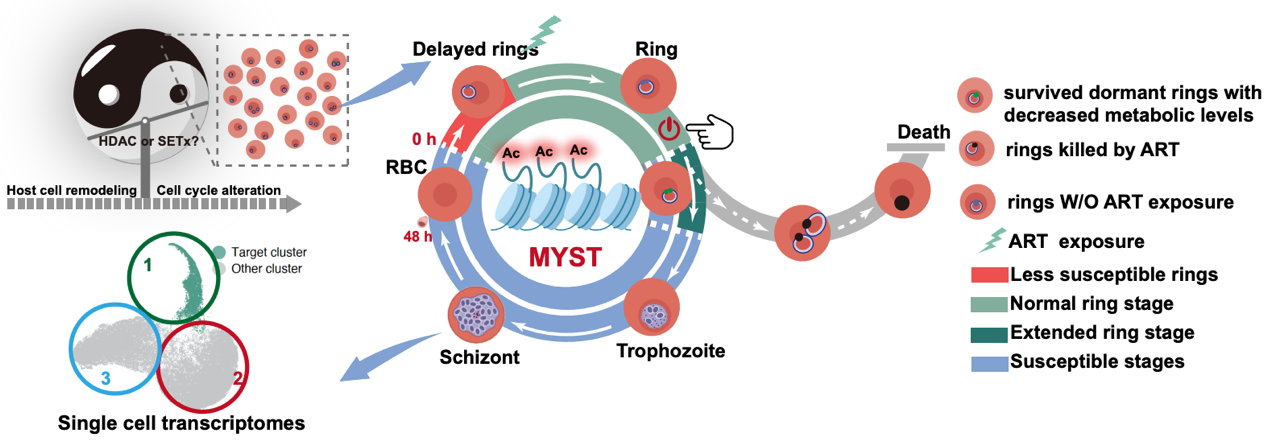
疟原虫感染引发的疟疾是全球最致命的传染病之一,每年全球发病人数达2亿以上,死亡60余万人。目前,青蒿素及其衍生物(如双氢青蒿素)是当前最有效的抗疟药物核心成分。青蒿素联合疗法(ACT)是目前疟疾治疗的一线方案,但药物在体内半衰期较短。研究发现,少量红细胞内的环状期疟原虫会进入一种“休眠状态”,暂时停止代谢活动,躲过青蒿素药物攻击。若联合用药未能清除这些“漏网之鱼”,它们便会苏醒并导致疾病复发。更棘手的是,部分疟原虫通过PfK13基因突变获得了更强的休眠能力,其环状期存活率超过1%时,即被定义为“青蒿素部分耐药性”。但仅靠基因突变无法完全解释这一现象,暗示了表观遗传调控可能才是关键。
研究团队对73株疟原虫临床分离株进行了系统性分析,重点关注了一类可能调控基因表达的组蛋白乙酰转移酶。结果发现,只有PfMYST的表达与环状期存活率完全关联。当乙酰转移酶PfMYST被抑制时,疟原虫的休眠能力显著下降,反之则增强。通过单细胞RNA测序和基因编辑技术,团队进一步锁定了PfMYST调控的靶基因,并发现它与已知的耐药相关蛋白PfK13存在相互作用。这意味着,疟原虫可能通过PfMYST的表观遗传修饰和PfK13的基因突变双管齐下,激活休眠程序,逃避免疫系统和药物追杀。这项研究首次揭示了表观遗传在疟原虫耐药性中的核心作用,不仅为青蒿素抗性干预提供了理论指导,也为开发新型抗疟药提供了关键靶点。
该研究得到了国家重点研发计划(2023YFA1801004)、国家自然科学基金(82230077、W2411080、82320108014、81971967、82102424)等项目的支持。
稿件来源:基础医学院
稿件审核:周洁 张青锋
责任编辑:陈曦

